ENDO-VAC
ENDO-VAC therapy: Vacuum Assisted Closure Therapy endoscopica per trattamento di ascessi extraluminali
La V.A.C. Therapy (Vacuum Assisted Closure Therapy) viene presentata nel 1995 dalla Kinetic Concepts per trattare con pressione negativa ferite altrimenti di difficile gestione. La sua applicazione alla endoscopia, ossia l’ENDO-V.A.C. therapy viene invece descritta nel 2000 da Grutzmar e Weidanhagen per il trattamento di deiscenze anastomotiche colorettali applicando i medesimi concetti. Il principio è quello delle macro e micro-deformazioni. Le macro-deformazioni permettono un migliore avvicinamento dei lembi con aspirazione di essudato infetto e secrezioni. Le micro-deformazioni danno uno stimolo cellulare recettoriale di rinnovamento e precoce rigenerazione.

Fig. 1 – Evidenza di comunicazione fra raccolta ascessuale pelvica e cavità peritoneale, verosimile esito di posizionamento di drenaggio chirurgico
Indicazioni
L’indicazione più promettente per l’Endo-SPONGE è sicuramente il trattamento precoce degli ascessi para-anastomotici pre-sacrali che seguono le deiscenze anastomotiche a seguito di resezione di retto. Questa rappresenta un’importante causa di morbidità e mortalità, di difficile trattamento.
Iter diagnostico pre-trattamento
È sempre necessario eseguire una TC pre-endoscopia per distinguere ascessi pelvici da raccolte endo-addominali che controindicano la procedura per il rischio di peritonite diffusa. È inoltre necessario escludere dal trattamento i casi nei quali sia presente un tramite fistoloso che metta in comunicazione la cavità da trattare con il cavo peritoneale, come è sovente il caso in presenza di drenaggio chirurgico para-anastomotico (Fig. 1). Rappresentano inoltre controindicazioni al trattamento la presenza di vasi sanguigni a diretto contatto con l’Endo-SPONGE ed il diretto contatto di parti di piccolo e grosso intestino al dispositivo, per il rischio di erosione.
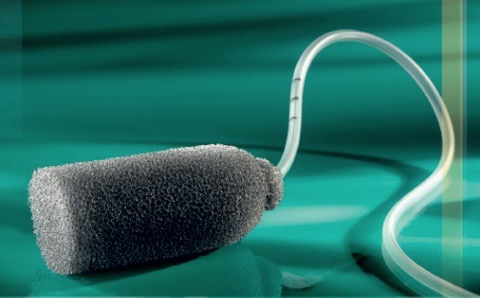
Fig. 2 – Endo-SPONGE
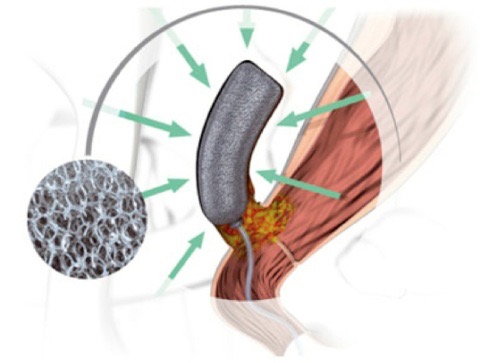
Fig. 3 – La pressione esercitata si distribuisce equamente a tutta la superficie dell’Endo-SPONGE e di conseguenza al tessuto in contiguità con esso
Metodica
Lo strumento Endo-SPONGE (B. Braun, Germania) è formato da una spugna di poliuretano dotata di pori da 400 a 600 micron e dalle dimensioni standard, ma sagomabili, di 7 cm di lunghezza e 3 cm di diametro, connessa a un tubo di drenaggio per poter mantenere il sistema in aspirazione (Fig. 2). La pressione esercitata si distribuisce equamente a tutta la superficie dell’Endo-SPONGE e di conseguenza al tessuto in contiguità con esso (Fig. 3). Il posizionamento del dispositivo viene eseguito sotto guida endoscopica in modo da poter valutare in toto la lesione con relative misure (distanza dal margine anale e dimensioni della cavità). Qualora l’orifizio per accedere alla cavità fosse tale da non consentire il passaggio dello strumento endoscopico, si renderebbe necessario eseguire una dilatazione endoscopica con pallone dilatatore fino a un calibro di almeno 15 mm. Una volta avuto accesso alla cavità, si esegue una abbondante detersione con soluzione fisiologica e iodata. Quindi, sulla guida dell’endoscopio introdotto all’interno della cavità, si fa scivolare all’interno della stessa il tubo introduttore. Rimosso l’endoscopio, la spugna imbibita di gel idrico viene spinta nell’introduttore con un apposito strumento spingitore. Una volta che la spugna è introdotta nella cavità, si ritirano introduttore e spingitore facendo attenzione a lasciare nella cavità la spugna con il tubo di drenaggio. Dopo un controllo endoscopico del posizionamento (Fig. 4) si procede al collegamento del tubo di drenaggio del sistema V.A.C. al sistema di aspirazione. Tutto il sistema diviene quindi automaticamente ermetico senza necessità di ulteriori accorgimenti. Se ciò non dovesse verificarsi è necessario procedere a un nuovo posizionamento del dispositivo. Il dispositivo è disegnato per rimanere in sede 48-72h, dopodiché si procede alla sua sostituzione. Per fare ciò è necessario eseguire un abbondante lavaggio attraverso il tubo di drenaggio connesso alla spugna, con soluzione fisiologica, di modo da liberare la spugna dalle aderenze con il tessuto che riveste la cavità al suo interno. Nell’eseguire tale manovra è necessario inoltre esercitare una lieve trazione del sistema, il tutto sotto controllo endoscopico. È possibile osservare modesti sanguinamenti autolimitantisi dopo tale manovra. Si verifica il corretto granuleggiamento della superficie della cavità (Fig. 5). Si deterge quindi con ulteriore soluzione fisiologica e iodopovidone la cavità prima di inserire un nuovo dispositivo.
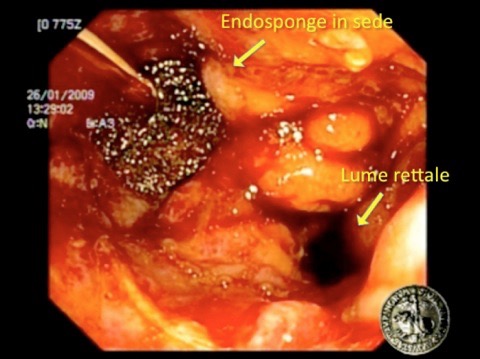
Fig. 4 – Controllo endoscopico del posizionamento
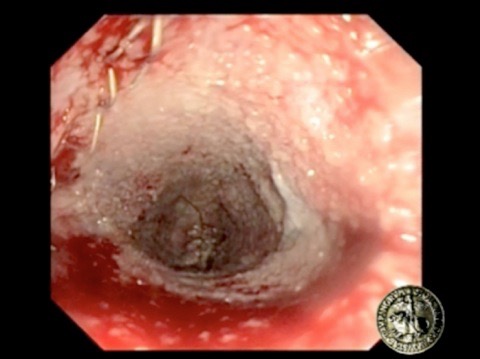
Fig. 5 – Corretto granuleggiamento della superficie della cavità
Gestione del paziente
Il trattamento minimo necessario perché la procedura abbia effetto si è rivelato essere di 4 settimane. Durante la terapia non è sempre necessaria una copertura antibiotica e il paziente non avverte in genere dolore. Quando la cavità è di dimensioni < 1 cm di diametro e < 5 mm di profondità, questa si può considerare guarita (Fig. 6), e tende a riepitelizzarsi a mo’ di pseudo-diverticolo. Tuttavia nelle fasi iniziali di trattamento è possibile che si renda necessario un intensivo supporto nutrizionale, parenterale se il paziente non è portatore di enterostomia escludente a monte. Analogamente per un miglior controllo della sepsi, può essere necessaria una copertura antibiotica ad ampio spettro per prevenire sepsi locale e quindi sistemica. L’esecuzione di una enterostomia se non già presente, non è sempre necessaria, ma può diventarlo se è necessario un miglior controllo della sepsi locale.
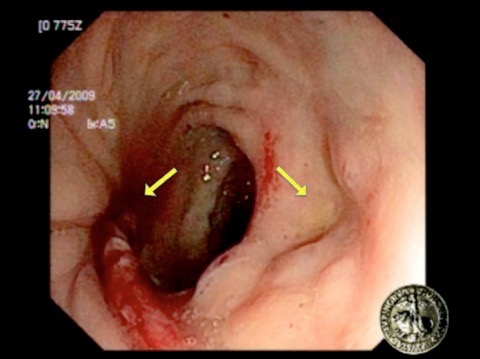
Fig. 6 – Esempio di cavità ascessuale completamente guarita dopo 4 settimane
Il ricovero per questo trattamento raramente è necessario, se non nelle prime fasi, quando sono presenti esiti chirurgici recenti; nella maggior parte dei casi si seguirà il paziente ambulatorialmente. Questa decisione viene presa in base al rischio connesso al paziente stesso e in particolare è legato all’altezza della lesione, alle dimensioni della cavità e alla percentuale di circonferenza interessata dalla deiscenza (1,2). La eventuale precedente radioterapia influisce negativamente sul successo di questa metodica, mentre le patologie benigne trattate hanno avuto invece un 100% di successo. Va inoltre detto che la metodica si è dimostrata più efficace nel trattamento di ascessi in fase acuta. Questo è dovuto al fatto che un tessuto fibrotico come da ascesso inveterato è meno portato alla granulazione percui è richiesto un trattamento più prolungati (3). La percentuale di guarigione totale è di circa il 90% (4). Nelle lesioni restie alla guarigione si può procedere all’iniezione di colla di fibrina con beneficio (5).
Bibliografia
- Mees ST, Palmes D, Mennigen R, Senninger N, Haier J, Bruewer M. Endo-vacuum assisted closure treatment for rectal anastomotic insufficiency. Dis Colon Rectum. 2008 Apr;51(4):404-10
- Arezzo A, Miegge A, Garbarini A, Morino M. Endoluminal vacuum therapy for anastomotic leaks after rectal surgery. Tech Coloproctol 2010; Sep;14(3):279-81. Epub 2010 Mar 30)
- van Koperen PJ, van Berge Henegouwen MI, Rosman C, Bakker CM, Heres P, Slors JF, Bemelman WA. The Dutch multicenter experience of the endo-sponge treatment for anastomotic leakage after colorectal surgery. Surg Endosc. 2009 Jun;23(6):1379-83. Epub 2008 Nov 27
- Weidenhagen R, Gruetzner KU, Wiecken T, Spelsberg F, Jauch KW. Endoluminal vacuum therapy for the treatment of anastomotic leakage after anterior rectal resection. Rozhl Chir. 2008 Aug;87(8):397-402
- Glitsch A, von Bernstorff W, Seltrecht U, Partecke I, Paul H, Heidecke CD. Endoscopic transanal vacuum-assisted rectal drainage (ETVARD): an optimized therapy for major leaks from extraperitoneal rectal anastomoses. Endoscopy. 2008 Mar;40(3):192-9